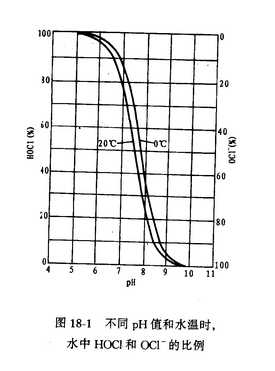
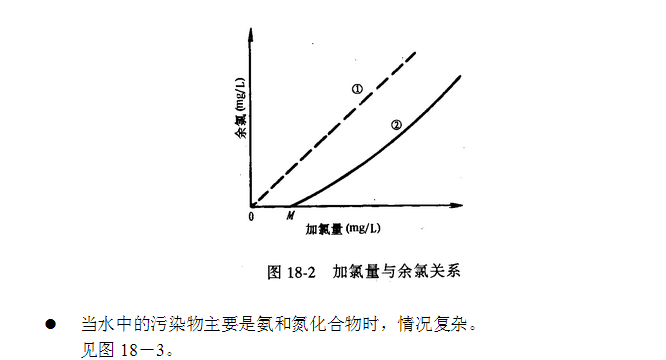
余氯:出廠水接觸30分后余氯不低于0.3mg/L;在管網末梢不應低于0.05mg/L,。 加氯曲線: ? 水中無任何微生物,、有機物等,加氯量=余氯,,圖18-2中的① ? 水中有機物較少時,,需氯量滿足以后就是余氯。圖18-2中的②
1. 加氯設備
一般用氯氣:有毒氣體,,在6-8氣壓下變成液氯 使用時采用氯瓶。干燥氯氣和液氯對鋼瓶無腐蝕作用,,但遇水或受潮則會嚴重腐蝕金屬,。因此,必須嚴格防止水和潮氣進入氯瓶,。 加氯機:轉子加氯機#p#分頁標題#e#

六,、氯化消毒副產物
有機物與氯生成有機氯化物,三鹵甲烷,。
我G新標準規(guī)定了三鹵甲烷(THMs)濃度,,包括:氯仿、溴仿,、二溴一氯甲烷和一溴二氯甲烷四種物質,。
1993年美G制訂的消毒劑-消毒副產物方案中建議: THMs 80 ?g/L,
鹵乙酸(HAAS):一共五種(一氯乙酸,、二氯乙酸,、三氯乙酸,、一溴乙酸、二溴乙酸),,五種之和在1997年低于60 ?g/L,,2000年低于30?g/L。
第3節(jié) 其它消毒法
一,、氯氨消毒
優(yōu)點:水中含有有機物和酚時,,氯氨消毒不會產生氯臭和氯酚臭,大大減少了THMs的產生,,能保持水中余氯較久,。
但作用緩慢,殺菌能力比自由氯弱,。單獨使用的情況較少,。 人工投加氨可以是液氨,、硫酸氨或氯化氨,。
氯和氨的投加量視水質不同而有所不同。一般采用氯:氨=3:1~6:1 采用氯氨消毒時,,一般先加氨,,再加氯。
二,、二氧化氯消毒
ClO2在常溫下是一種黃綠色氣體,,具有刺激性。溶解度是氯的5倍,。極不穩(wěn)定,,氣態(tài)和液態(tài)ClO2均易爆炸。故必須以水溶液的形式現(xiàn)場制取,。 制取方法:
亞氯酸鈉和氯制?。?nbsp;
Cl2 + H2O → HOCl + HCl
HOCl + HCl +2NaClO2 → 2 ClO2 + 2NaCl +H2O
用酸與亞氯酸鈉制取:
5NaClO2 + 4HCl → 4 ClO2 + 5NaCl + 2H2O
ClO2既是消毒劑又是氧化能力很強的氧化劑。對細菌的細胞具有較強的吸附和穿透能力,,滅活能力強,。
不會與水中有機物作用生成有機氯化物。甚**本身的氧化能力能去除THMs前驅體,。
ClO2消毒能力比氯強,。
ClO2不水解,消毒受pH影響較小,。 ClO2余量能在管網中保持很長的時間,。 作為氧化劑,能去除或降低水的色度等,。
但ClO2本身和副產物ClO2-
對人體血紅細胞有損害,。有報道認為還對人的神經系統(tǒng)及生殖系統(tǒng)有損害,。
三、臭氧消毒
作用:既是氧化劑,,又是消毒劑,,滲入細胞壁。
作為消毒劑,,不會產生三鹵甲烷副產物,,殺菌和氧化能力比氯強。但由于臭氧在水中
不穩(wěn)定,,易散失,,因此在O3之后,往往需要投加少量的氯等,。
歐洲普遍用臭氧處理飲用水,,在美G也逐漸流行。 但近年來臭氧化的副作用也開始引起人們的關注,。
水中大分子物質變成分子較小的中間產物,,可能有毒性?;蛘咧虚g產物和氯作用后致
突變反而增強,。
四、其它
次氯酸鈉消毒:次氯酸鈉發(fā)生器食鹽電解:NaCl+H2O?NaOCl+H2?紫外線消毒:消毒速度快,,幾十秒鐘即能殺菌,;不影響水的物理和化學性質;操作簡單 電化學消毒:消毒效率高
第4節(jié) 污水消毒
污水經一級或二級處理以后,,水質大大改善,,細菌含量也幅度降低,但細菌的**值仍很高,,并存在有病原菌的可能,。因此在排放之前或回用之前,應進行消毒,。
.